1 引言
砷是一种毒性很高的原生质毒物,与汞、镉、铬、铅被称为环境五毒,砷及其化合物是常见的环境污染物,其污染危害已经成为一个全球性问题。砷在环境中以有机砷和无机砷两种形态存在,但在天然水体中常以无机砷形态存在,无机砷主要以亚砷酸根离子(AsO2−)和砷酸根离子(AsO43−)形式存在于水中,其中As(III)比As(V)的毒性高出60倍。近年来,伴随着化工、采矿、冶炼、皮革、玻璃制造、农药、木材防腐剂及陶瓷等行业的快速发展,相当数量的砷随排出的工业废水进入环境中,特别是国内砷污染突发事件的频发,更引起社会各界的关注,例如2007年年底贵州省的独山县砷污染、都柳江砷污染及2008年云南阳宗海砷污染等。砷已被美国疾病控制中心(CDC)和国际癌症研究机构(IARC)确定为第一类致癌物质,许多国家也已把水中的砷列为优先控制的污染物之一。
目前含砷废水的处理技术主要有化学沉淀法、絮凝沉淀法、铁氧体法、离子交换法、电渗析法、膜分离法、光催化氧化法、吸附法、微生物胞内转化法、微生物胞外转化法、微生物死细胞吸附法、植物吸收法及活性污泥法等,现有处理技术均存在不足之处,其中吸附法适用于低浓度含砷废水,含砷吸附材料的堆存要求苛刻;电凝聚法操作复杂,能耗大,设备腐蚀严重;离子交换法对复杂废水交换树脂易失效,成本过高;铁氧体法能耗高;电渗析法目前尚处于实验室阶段;生化法存在固定资本较高等问题。因此开发技术成熟、成本低廉及高效可靠的高浓度含砷废水处理技术刻不容缓。
高铁盐是六价铁的含氧酸盐,是一种绿色高效的具有选择氧化性的水处理药剂,兼具氧化、絮凝、消毒、杀菌多种功能,近年来在水处理领域得到广泛关注。高铁盐具有极强的氧化性,在酸、碱性条件下的氧化还原电位分别为+2.20V和+0.72V,所以有极强的氧化除污能力。高铁盐溶于水后,Fe(VI)经过中间价态逐渐被还原成Fe(III),期间会产生具有比铝盐和铁盐的水解产物更高的正电荷及更大的网状结构的正价态水解产物,可吸附各种阴阳离子及重金属离子,以达到净水的目的。然而,高铁盐制备工艺复杂,稳定性差,目前仍缺乏大规模生产及应用的较完善工艺数据,因此有必要发展高铁盐联用技术除砷。而MSC具有独特的纳米尺度微孔及层间结构,比表面积大,对重金属离子吸附能力强,基于K、Na取代的水化C-S-H具有很高的阳离子交换容量,C-S-H相可将重金属稳定固化在其晶格内部,MSC是一种高效能、低成本且能长时间对重金属离子有效固化或转化的活性材料。因此,本文采用高铁预氧化-MSC联用法除砷,取得了较高除砷率的同时也降低了除砷剂耗量,为高浓度含砷废水的高效处理提供了新思路。
2 实验
2.1 试剂与材料
研究所用的主要材料矿物基土壤调理剂为根据专利自主研制,试剂硫酸,氢氧化钠,冰乙酸,三水合乙酸钠,高铁盐,亚砷酸钠,均为分析纯。模拟含砷废水以亚砷酸钠与蒸馏水配制而成,砷浓度为500.0mg/L,pH值10.60。
2.2 实验仪器
AEY220型分析天平,HCJ-6D恒温水浴磁力搅拌器,PHS-3C型pH计,AFS-9130型原子荧光光谱仪。
2.3 实验方法
将浓度为500.0mg/L含砷废水转移至一系列500mL的玻璃烧杯,加入一定量的除砷剂,先以300r/min的转速快速搅拌5min,再以130r/min的转速搅绊15min,之后用10%的硫酸和0.1mol/L的氢氧化钠调节pH值,控制一定的温度,以130r/min的转速搅拌一定时间,静置30min。取上清液,用国家标准方法原子荧光光谱法测定水样的含砷量。
3 结果与讨论
3.1 Fe/As摩尔比对除砷效果的影响
反应条件:反应温度25℃,改变高铁盐的投加量,氧化时间20min,调节pH值为7.0,反应时间为60min,静置过滤。实验结果如图1所示。
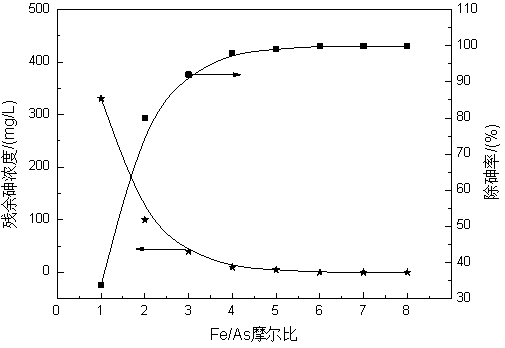
图1 Fe/As摩尔比对除砷效果的影响
图1表明,残余砷浓度随着Fe/As摩尔比增加呈先减小后逐渐趋于稳定的趋势。在Fe/As摩尔比低于6时,残余砷浓度较高,主要是因为高铁盐的加入量少,不足以使三价砷充分氧化为五价砷,As(III)在pH<9.5时处于非离子状态,表现出电中性,絮凝、沉淀、吸附等对As(V)脱除是很有效的方法,而对As(III)却收效甚微,从而导致除砷率低。在Fe/As摩尔比为6时,残余砷浓度达到《污水综合排放标准》(GB8978)第一类污染物排放标准(0.5mg/L),砷的脱除效果较好,再增加Fe/As 摩尔比对除砷效果影响很小。
3.2 MSC/As质量比对除砷效果的影响
反应条件:反应温度25℃,改变MSC的投加量,调节pH值为7.0,反应时间为60min,静置过滤。实验结果如图2所示。
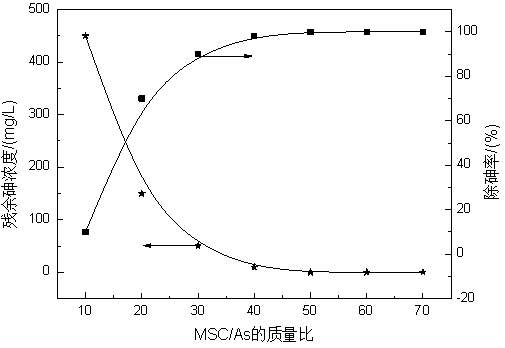
图2 MSC/As质量比对除砷效果的影响
由图2可知,随着MSC/As质量比增加,残余砷浓度先减小后逐渐趋于稳定。这与矿物基土壤调理剂的特性密切相关,矿物基土壤调理剂具有独特纳米尺度的微孔及层间结构,比表面积可达44~49m2/g,基于K、Na取代的水化C-S-H具有很高的阳离子交换容量,水化C-S-H相属纳米层间晶体结构,对砷等重金属离子具有强烈的物理化学吸附作用,可有效脱除砷等重金属离子,在MSC/As质量比小于50时,由于所用的矿物基土壤调理剂的阳离子交换容量和物理化学吸附已基本达到饱和状态,无法对残余砷起到脱除作用,从而使残余砷浓度较高,随着MSC/As质量比增加,矿物基土壤调理剂的阳离子交换容量和物理化学吸附能力相应增加,除砷率逐渐增加,在MSC/As质量比为50时,已达到较高除砷率,再增大MSC/As质量比对除砷率影响不大。
3.3 高铁预氧化-MSC联用法对除砷效果的影响
由上述讨论可知,高铁法与矿物基土壤调理剂法的除砷机理不同,高铁酸盐除砷时,可先将三价砷氧化为五价砷,再通过多相聚合作用除砷;而矿物基土壤调理剂的除砷机理是基于其阳离子交换容量和物理化学吸附能力,除砷率虽然不受As3+与As5+浓度的制约,但对As5+的去除效果要远大于对As3+的去除效果。对比图1和图2可知,高铁酸盐法的除砷效果优于矿物调理剂法,产生的污泥量也较矿物调理剂法少,但矿物基土壤调理剂在成本及过滤性能方面有很大优势。经综合考虑,采用高铁预氧化-MSC联用法进行除砷研究。
反应条件:反应温度25℃,改变除砷剂的投加量,调节pH值为7.0,反应时间为60min,静置过滤。实验结果如图3所示。
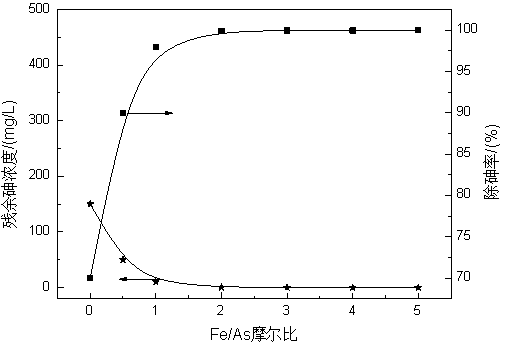
图3 高铁预氧化-MSC联用法对除砷效果的影响
图3表明,在MSC/As质量比为20的情况下,随Fe/As摩尔比增加,残余砷浓度呈先减小后逐渐趋于稳定的趋势。在Fe/As摩尔比为2时,残余砷浓度就可达到污染物排放标准(0.5mg/L)。而分别采用单纯的高铁盐和矿物基土壤调理剂除砷时,所需投加量分别为Fe/As摩尔比为6和MSC/As质量比为50。这是因为含砷废水中没有投加高铁盐时,砷以三价态砷化合物形式存在于废水中,而矿物基土壤调理剂对As3+的去除效果相对不理想,此时除砷率不太高;在含砷废水中投加高铁盐后,具有强氧化性的高铁盐可将三价砷迅速氧化为五价砷,而矿物基土壤调理剂对As5+的去除效果要远大于对As3+的去除效果,且高铁盐的还原产物又可用于后续絮凝除砷,高铁预氧化-MSC协同作用明显,显著提高了除砷率;随着Fe/As摩尔比增加,三价砷的氧化率逐渐增加,除砷率相应增加;在Fe/As摩尔比为2时,三价砷已被充分氧化为五价砷,除砷率基本达到稳态,再增加Fe/As摩尔比,对除砷率影响极小,反而使除砷成本增加。因此,选取除砷剂的最佳用量为Fe/As摩尔比为2和MSC/As质量比为20。
3.4 pH值对高铁预氧化-MSC联用法除砷效果的影响
反应条件:反应温度25℃,Fe/As摩尔比为2,MSC/As质量比为20,改变pH值,反应时间为60min,静置过滤。实验结果如图4所示。
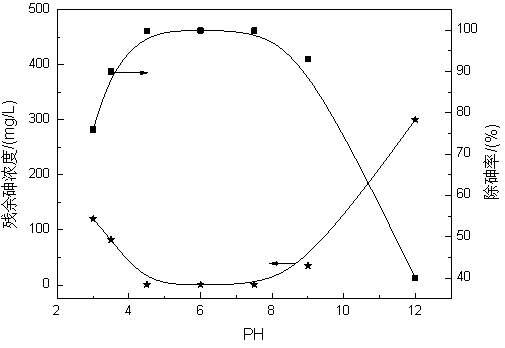
图4 pH值对高铁预氧化-MSC联用法除砷效果的影响
高铁酸盐的稳定性、氧化絮凝效果及矿物基土壤调理剂除砷效果受pH值影响很大,因此pH值的控制就显得十分重要。由图4可知,pH值在5.5~7.5范围时,残余砷浓度出现最小值0.5mg/L,随pH值增加,残余砷浓度迅速增加。究其原因可能为:
(1)由FeO42-氧化H3AsO3的微电池反应知,在高pH条件下,H3AsO3平衡浓度大,残余砷浓度相应增加。
(2)Fe3+离子在高pH条件下主要以 Fe(OH)3(s)及Fe(OH)4−等羟合铁离子形态存在,促使反应生成的非晶形砷酸铁反溶。
(3)矿物基土壤调理剂内的C-S-H相可将五价砷稳定固化在其晶格内部,对五价砷具有强烈的物理化学吸附作用,随着pH增加,C-S-H相表面带更多的负电荷,静电作用即排斥作用力增加,导致对砷的物理化学吸附能力降低。
(4)MSC的制备所采用的主要原料为天然活性铝硅酸盐矿物,由XRD图谱分析知,活性铝硅酸盐中包含有18.51% Al2O3,根据相关文献资料:在pH值为5~6时,活性氧化铝对砷(V)去除效果最好,在pH值为7~8时,活性氧化铝对(III)去除效果最好,随着pH值的继续增加,活性氧化铝的溶解度增加,进而造成其吸附效率降低而释放出砷。由图5还看到,pH<5.5时,残余砷浓度也较大,这可能是由于:低pH条件下,非晶形砷酸铁稳定性降低,发生了反溶现象,致使除砷率降低,该结果与文献报道的相一致;低pH值时使得废水中H2AsO3-、HAsO32-及AsO33-减小,大部分以H3AsO3的形态存在,表现出电中性,不能通过静电作用被絮凝吸附;此外,活性氧化铝在pH<4时溶解度增加,也会造成除砷率的降低。因此pH值在5.5~7.5范围时,高铁预氧化-MSC联用法除砷效果最好,选取最佳pH值为7。
3.5 反应时间对高铁预氧化-MSC联用法除砷效果的影响
反应条件:反应温度25 ℃,Fe/As摩尔比为2,MSC/As质量比为20,pH值为7,改变反应时间,静置过滤。实验结果如图5所示。
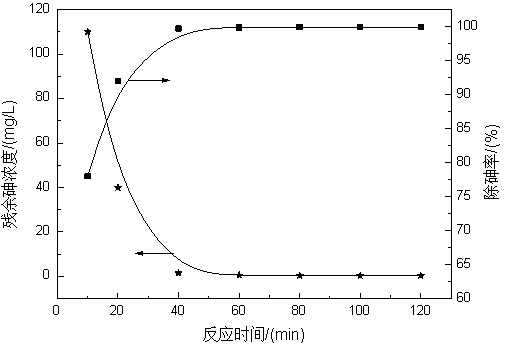
图5 反应时间对高铁预氧化-MSC联用法除砷效果的影响
图5表明,除砷率在反应时间为0~40min内迅速增加,随着反应时间的增加,除砷率在反应时间为40~60min内缓慢增加,当反应时间为60min时除砷率基本趋于稳定。造成在这种现象的原因可能为:在含砷废水中投加高铁盐后,由于Fe(VI)与As(III)反应的半周期为1s,高铁盐与As(III)的氧化反应可在很短的时间内完成,与此同时,其还原产物通过多相凝聚作用快速脱除砷,而在矿物基土壤调理剂除砷的初始阶段,由于As(V)浓度在废水和矿物基土壤调理剂表面相差较大,吸附推动力较大,因而能迅速地被吸附在矿物基土壤调理剂表面,除砷率较大;随着反应时间延长,废水和矿物基土壤调理剂两相间浓度差逐渐降低,吸附阻力逐渐增大,再加上矿物基调理剂表面的As(V)向其微孔内部扩散的速率较缓慢,使得吸附效率减缓,除砷率逐渐趋于稳定。本研究选取60 min为最佳反应时间。
3.6 温度对高铁预氧化-MSC联用法除砷效果的影响
反应条件:改变反应温度,Fe/As摩尔比为2,MSC/As质量比为20,pH值为7,反应时间为60min,静置过滤。实验结果如图6所示。
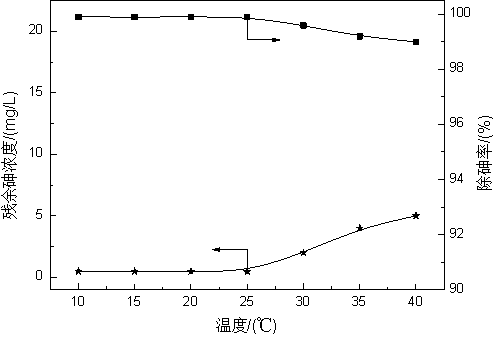
图6 温度对高铁预氧化-MSC联用法除砷效果的影响
由图6可知,在温度低于25℃时,残余砷浓度较低,温度对除砷率影响不大;当温度高于25℃时,残余砷浓度随着温度增加而缓慢增加。这是因为:随着温度增加,高铁盐在废水中的稳定性随之降低,As(III)的氧化率也相应降低,进而造成除砷率的降低;同时非晶形砷酸铁的溶解度随温度增加而增大,故废水中的残余砷浓度增加;另外在矿物基调理剂除砷过程中,在低温区阶段,温度对As(V)在矿物基调理剂表面及孔道内的扩散和吸附作用影响不大,使得除砷率基本不变,随着温度增加,砷的扩散速率随之增加,使矿物基调理剂发生脱附现象,进而造成残余砷浓度增加。因此,本实验选取25 ℃为最佳反应温度。
4 结论
(1)高铁预氧化-MSC钝化联用法处理含砷模拟废水,高铁预氧化-MSC联用法除砷具有工艺简单、投资少、除砷效果好及无次生污染等优点。最佳工艺条件为:反应温度25℃,Fe/As摩尔比为2,MSC/As质量比为20,pH值为7,反应时间60min。
(2)与单纯的高铁盐法和矿物基土壤调理剂法相比,高铁预氧化-MSC联用法使除砷率得到显著提高,高铁盐及MSC的用量大大降低,且运行成本也相应降低。
(3)采用高铁预氧化-MSC联用法除砷,处理后水样中的残余砷浓度可达到《污水综合排放标准》(GB8978)第一类污染物排放标准(0.5mg/L)的要求。
参考文献
[1]唐彬,邱亚群,胡立琼,等.含铁材料修复砷污染土壤的研究进展[J].安徽农业科学,2014,42(12).
[2]余芳.改性介孔分子筛吸附剂的制备与吸附除砷研究[D].长沙:中南大学,2011.
[3]Wang Xiaowei,Xi Beidou,Huo Shouliang,et al.Investigation progress of membrance technology application to arsenic removal in drinking water[J].Technology of Water Treatment,2011,37(6).
[4]Zhang W,Singh P,Paling E,et al.Arsenic Removal fromContaminated Water by Natural Iron Ores[J].Miner. Eng.,2004,17(4).
[5]Zhihui Yang,Zijian Wu,Yingping Liao,et al.Combination of microbial oxidation and biogenic schwertmannite immobilization:A potential remediation for highly arseniccontaminatedsoil[J].Chemosphere,2017,(181).
[6]Zhang W,Singh P,Paling E,et al.Arsenic Removal fromContaminated Water by Natural Iron Ores [J].Miner. Eng.,2004,17(4).
[7]施建兵,林集先,邱凌峰.高铁酸盐在微污染源水除砷中的应用效果及其影响因素研究[J].能源与环境,2008,(1).
[8]Wood R H.The heat,free energy and entropy of the ferrate(VI) ion [J].J Am Chem Soc.,1958,(80).
[9]JiangJ Q,Lloyd B.Progress in the development and use of ferrate(VI) salt as an oxidant and coagulant for water and wastewatet treatment [J].Water Research,2002,(36).
[10]纪琼驰.高铁盐的制备及其在原水处理中的应用研究[D].南京:南京理工大学,2012.
[11]Hiroki Yoshida,Xu Gao,Shohei Koizumi,et al. Arsenic Removal from Contaminated Water Using the CaO–SiO2–FeO Glassy Phase in Steelmaking Slag[J].Sustain. Metall,2017,(3).
[12]刘耀驰,曹正海,钟楚彬.一种矿物基土壤修复剂及其制备方法.201610589686.1.
[13]蒋国民,王云燕,柴立元,等.高铁酸钾处理含砷废水[J].过程工程学报,2009,9(6).
[14]王强.麦饭石对腐殖酸及重金属离子的吸附作用[J].地质科技情报,1998,17(3).
[15]Rachana Singh,Samiksha Singh,Parul Parihar,et al.Arsenic contamination,consequences and remediation techniques: A review [J].Ecotoxicology and Environmental Safety,2015,(112).
[16]Lee Y,Um I,Yoon J.Arsenic(III) Oxidation by Iron(VI) (Ferrate)and Subsequent Removal of Arsenic(V) by Iron(III) Coagulation [J].Environ. Sci. Technol.,2003,37(24).
收稿日期:2018-04-08
作者简介:王程程(1988-),女,山东菏泽人,供职于湖南隆洲驰宇科技有限公司,硕士,研究方向:环境化学、矿物综合利用。刘耀驰(通信作者)(1972-),男,中南大学化学化工学院教授,研究方向:环境化学、功能材料及矿物综合利用。
基金项目:湖南省重点研发计划(项目编号:2016SK2069)。








